Vandenilio kuro elementų transporto priemonių veikimo principai
Vandenilio kuro elementų transporto priemonės (FCV) yra alternatyvaus kuro transporto priemonės, kurios kaip pagrindinį kuro šaltinį naudoja vandenilio dujas, kad gamintų elektrą per cheminį procesą kuro elemente. Šiose transporto priemonėse vandenilio dujos kaupiamos bakuose, o susijungus su deguonimi iš kuro elementų kamino oro, vyksta elektrocheminė reakcija, kurios metu gaminama elektra, kuria varomas transporto priemonės elektros variklis. Vienintelė šio proceso emisija yra vandens garai, todėl FCV yra perspektyvus sprendimas mažinant šiltnamio efektą sukeliančių dujų išmetimą ir oro teršalus transporto sektoriuje.
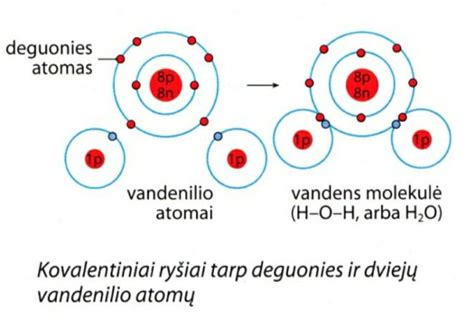
Kuro elemento struktūra ir elektrocheminė reakcija
- Vandenilio saugykla: FCV gabena vandenilio dujas laivo rezervuaruose.
- Kuro elementų kaminas: FCV širdis yra kuro elementų kaminas, kuriame yra keli atskiri kuro elementai.
- Elektrocheminė reakcija: Anode vandenilio dujos tiekiamos į kuro elementų kaminą, kur vyksta procesas, vadinamas vandenilio oksidacija. Vandenilio molekulės (H₂) skyla į protonus (H⁺) ir elektronus (e⁻).
- Elektrolitas: Anodo reakcijos metu susidarę protonai per elektrolito membraną patenka į katodą.
- Deguonis iš oro: Prie katodo deguonis (dažniausiai iš oro) susijungia su išorine grandine nukeliavusiais elektronais ir per elektrolitą praėjusiais protonais.
Akumuliatorių technologija ir oksidacijos reiškiniai
Akumuliatorius yra gyvybiškai svarbi transporto priemonės elektros sistemos dalis. Tarp visų aplinkos veiksnių temperatūra turi didžiausią įtaką akumuliatoriaus įkrovimui ir iškrovimui. Elektrocheminė reakcija elektrodo ir elektrolito sąsajoje yra tiesiogiai susijusi su aplinkos temperatūra.
Temperatūros įtaka elektrocheminiams procesams
Jei temperatūra nukrenta, elektrodo reakcijos greitis mažėja, o baterijos galia krinta. Aukšta temperatūra (virš 45°C) gali sunaikinti akumuliatoriaus cheminę pusiausvyrą ir sukelti nepageidaujamas šalutines reakcijas. Ličio jonų akumuliatoriuose, jei įkrovimas vyksta itin žemoje temperatūroje, metalinis litis gali ištirpti ant anodo paviršiaus - šis procesas yra negrįžtamas ir mažina saugos koeficientą.
Ličio baterijų tipai ir cheminė pusiausvyra
| Akumuliatoriaus tipas | Teigiamas elektrodas (katodas) | Neigiamas elektrodas (anodas) |
|---|---|---|
| Ličio jonų | Ličio lydinio metalo oksidas | Grafitas |
| Ličio metalo | Mangano dioksidas | Metalinis litis |
Akumuliatorių gnybtų oksidacija: priežastys ir prevencija
Akumuliatoriaus gnybtų oksidacija - tai cheminis procesas, kurio metu metaliniai paviršiai reaguoja su aplinkos veiksniais (deguonimi, drėgme). Tai sukelia apnašų susidarymą, didina elektros pasipriešinimą ir gali lemti sistemos gedimus.
Pagrindinės oksidacijos priežastys:
- Vandenilio dujų nuotėkis: Nepakankamas sandarumas įkrovimo metu.
- Elektrolito nutekėjimas: Agresyvios medžiagos korozija.
- Aplinkos veiksniai: Aukšta drėgmė ir temperatūros svyravimai.
Norint išvengti oksidacijos, patariama reguliariai tikrinti gnybtus, valyti juos silpnu sodos tirpalu ir po valymo tepti specialiu apsauginiu tepalu ar techniniu vazelinu, kuris apsaugo nuo drėgmės patekimo.
Išvalykite AKUMULIATORIŲ KOROZIJĄ nuo ELEKTRONIKOS PRIETAISŲ! LENGVAS „PASIDARYK PATS“! | 2 minučių pamokos, 4 serija
tags: #ekektrochemine #reakcija #oksiduojasi #akumuliatoriaus #laikikliai
