Katalizė - tai cheminės reakcijos greitinimas tam tikromis medžiagomis, vadinamomis katalizatoriais.
Jei cheminę reakciją greitina per reakciją susidaręs tarpinis arba galutinis produktas, katalizė vadinama autokatalize.
Pagal katalizuojamos sistemos fazinę būseną skiriama homogeninė (reaguojančių medžiagų ir katalizatoriaus fazės tokios pat) ir heterogeninė (reaguojančių medžiagų ir katalizatoriaus fazės skirtingos) katalizė. Pagal katalizuojamos cheminės reakcijos pobūdį gali būti rūgščių ir bazių, jonų mainų, oksidacijos ir redukcijos, polimerizacijos katalizė.
Jei katalizė vyksta katalizatoriui pernešant vieną iš reaguojančių medžiagų iš vienos fazės į kitą (pvz., iš skysčio į skystį, iš kietosios medžiagos į skystį), kurioje ji reaguoja su kita toje fazėje esančia medžiaga, katalizė vadinama tarpfazine.
Homogeninės katalizės katalizatorius yra dujos arba tirpalo komponentas, heterogeninės - dažniausiai kieta medžiaga (abiem atvejais katalizė vyksta dujose arba tirpaluose).
Katalizė apibūdinama jos metu savaime vykstančiomis katalizinėmis reakcijomis (greitis priklauso nuo katalizės pobūdžio ir katalizatoriaus veiksmingumo). Jos dažniausiai sudėtingesnės už paprastąsias: turi daugiau pakopų, gali vykti panašiai kaip grandininė reakcija (aktyvusis centras sukelia kitimų grandinę).
Katalizė lėmė šiuolaikinės chemijos pramonės atsiradimą, nes beveik visi chemijos technologiniai procesai yra kataliziniai, pvz., sieros ir azoto rūgščių bei amoniako gamyba, naftos perdirbimas, vienų organinių junginių sintezė iš kitų (etileno oksidavimas iki etilenoksido, metanolio - iki formaldehido, propileno - iki akrilaldehido).
Katalizė taikoma gaminant polietileną, polipropileną ir kitas polimerines medžiagas, šalinant dujinius teršalus, susidarančius deginant kurą, eksploatuojant automobilius, gaminant kai kurias medžiagas.
Katalizė pradėta tirti 19 a. pradžioje, atradus azoto oksidų katalizinį poveikį sieros dioksido oksidacijai iki sieros trioksido. Katalizės terminą 1835 m. pasiūlė J. J. Berzelius, kuris taip pat apibendrino iki to laiko gautus katalizės tyrimo rezultatus.
Fermentai - biologiniai katalizatoriai
Fermentai (lot. fermentum - rūgimas), dar vadinami enzimais, tai specifiniai baltymai, kurių turi visos gyvosios ląstelės. Jie atlieka biologinių katalizatorių vaidmenį.
Fermentų pagalba yra realizuojama genetinė informacija ir vykdoma medžiagų bei energijos apykaita gyvuosiuose organizmuose. Be fermentų šios reakcijos nevyktų arba vyktų labai lėtai, ir organizmai negalėtų egzistuoti.
Fermentai gali būti paprastieji ir sudėtiniai, kurių sudėtyje, be baltyminio komponento (apofermento), yra dar ir nebaltyminė dalis - kofermentas. Kai kurie fermentai, be aktyviųjų centrų, turi ir papildomų, taip vadinamų alosterinių reguliuojančių centrų.
Fermentų veikimo efektyvumą lemia žymus katalizuojamos reakcijos energijos aktyvacijos sumažėjimas tarpinių fermentų-substratinių kompleksų susidarymo rezultate. Substratų prisijungimas vyksta aktyviosiose centruose, kurie yra panašūs tik į tam tikrus substratus, kuo pasiekiama išskirtinė fermentų veikimo specifika. Viena fermentų ypatybių - tai sugebėjimas reguliuojamai ir kryptingai veikti. Jo sąskaita yra kontroliuojama visa medžiagų apykaitos grandžių darna.
Šį sugebėjimą nulemia fermentų struktūrinės molekulės erdviškumas. Jis realizuojamas per fermentų veikimo greičio kitimus ir priklauso nuo tam tikrų substratų ir kofaktorių koncentracijos, pH terpės, temperatūros, o taip pat nuo specifinių aktyvatorių ir inhibitorių (pvz. adenilo nukleotidų, karbonilinių, sulfhidrilinių junginių ir kt.) egzistavimo.
Fermentų biosintezę kontroliuoja genai. Skiriami konstitutyviniai (pastoviai esantys ląstelėse) ir indukuojami fermentai, kurių biosintezė aktyvuojasi veikiant atitinkamiems substratams. Kai kurie funkcionaliai tarpusavyje susiję fermentai ląstelėje sudaro struktūriškai organizuotus polifermentinius kompleksus.
Dauguma fermentų ir fermentinių kompleksų yra glaudžiai susiję su ląstelės membranomis ir jos organoidais (mitochondrijomis, lizosomomis, mikrosomomis ir t.t.) ir dalyvauja aktyviame medžiagų transportavime per membranas.
Žinoma daugiau kaip 20000 įvairiausių fermentų, daugelis kurių yra išskirti iš gyvųjų ląstelių ir gauti natūralioje būklėje. Pirmąjį kristalinį fermentą (ureazę) išskyrė amerikiečių biochemikas D. Sumneris 1926 metais. Kai kurių fermentų yra išanalizuota aminorūgščių seka, išaiškintas polipeptidų grandinių išsidėstymas trimatėje erdvėje. Laboratorijos sąlygomis įvykdyta dirbtinė cheminė ribonukleazės fermento sintezė.
Fermentai naudojami įvairių medžiagų kiekiui nustatyti ar išgauti, nukleino rūgšties molekulių modifikacijai genų inžinerijos metodais, eilės susirgimų diagnostikai ir gydymui, taip pat eilėje technologinių procesų, vykdomų lengvojoje, maisto ir farmacijos pramonėje.
Fermentų struktūra ir savybės
Kadangi fermentai yra baltymai, jie turi visas jiems būdingas savybes. Tuo pačiu biokatalizatoriai charakterizuojami eile specifinių savybių, esančių taip pat baltyminės prigimties. Šios savybės skiria fermentus nuo paprasto katalizatoriaus.
Termolabilumas
Fermentų termolabilumas paaiškinamas tuo, kad temperatūra veikia fermento baltyminę dalį, kas, esant aukštai temperatūrai, lemia baltymo denatūraciją ir katalitinės funkcijos sumažėjimą. Kita vertus, tai lemia fermentų-substratų komplekso susidarymo reakcijos greitį ir visus sekančius substrato kitimo etapus, kas lemia katalizės sustiprėjimą.
Fermento katalitinio aktyvumo priklausomybė nuo temperatūros išreiškiama tipine kreive. Iki tam tikros atžymos (vidutiniškai iki 50°C) katalitinis aktyvumas auga, kas 10°C apytikriai 2 kartus išauga substrato kitimo greitis. Tuo tarpu palaipsniui auga inaktyvuoto fermento kiekis, jo baltyminės dalies denatūracijos sąskaita. Esant virš 50°C temperatūrai smarkiai padidėja fermentinio baltymo denatūracija, ir, nors substrato kitimų reakcijų greitis kyla, fermento aktyvumas, išreikštas pakitusio substrato kiekiu, krenta.
Temperatūra, prie kurios fermento katalitinis aktyvumas yra maksimalus, vadinama temperatūriniu optimumu. Skirtingų fermentų temperatūrinis optimumas yra nevienodas. Gyvulinės kilmės fermentų jis yra 40°-50°C, tačiau egzistuoja ir turintys aukštesnį temperatūrinį optimumą.
Priklausomybė nuo pH
Fermento priklausomybė nuo pH terpės reikšmės buvo nustatyta daugiau kaip prieš 50 metų. Kiekvienas fermentas turi savo optimalų pH, prie kurio pasireiškia jo maksimalus aktyvumas. Daugumos fermentų maksimalus aktyvumas pastebimas pH zonoje netoli neutralaus taško. Labai rūgščioje ar šarminėje terpėje gerai veikia tik kai kurie fermentai.
Perėjimas prie didesnės ar mažesnės (palyginus su optimalia) vandenilinių jonų koncentracijos sukelia fermento aktyvumo kritimą. Vandenilinių jonų koncentracijos įtaka katalitiniam fermentų aktyvumui pasireiškia jo aktyvaus centro poveikiu. Prie skirtingų pH reikšmių reakcinėje terpėje aktyvusis centras gali būti stipriau ar silpniau jonizuotas, daugiau ar mažiau priklausomas nuo kamyninių polipeptidų grandinės fermentų baltyminių dalių ir t.t. Terpės pH įtakoja substrato, fermentų-substratų komplekso, reakcijos produktų jonizacijos laipsnį, įtakoja fermento būseną, nustatant jame katijoninių ir anijoninių centrų sąveiką, kas veikia baltyminės molekulės struktūrą.
Specifiškumas
Specifiškumas - viena ypatingų fermentų savybių. Ši savybė buvo atrasta dar 19 a., kai buvo pastebėta, kad labai artimos struktūros substancijos - erdviniai izomerai (α- ir β-metilgliukozidai) yra skaidomi dviem visiškai skirtingais fermentais. Tokiu būdu fermentai gali atskirti cheminius junginius, besiskiriančius vieni nuo kitų nereikšmingomis struktūrinėmis detalėmis.
1950-aisiais metais statiškas įsitikinimas, kad fermento ir substrato atitikimas yra tikslus ir nekintantis, buvo pakeistas D. Košlando hipoteze apie indukuotą substrato ir fermento atitikimą. Jos esmė yra tame, kad erdvinis substrato ir fermento aktyvaus centro atitikimas susikuria jų tarpusavio sąveikos momentu, kas gali būti išreikšta formule: „pirštinė-ranka“. Tuo taru substrate jau deformuojasi kai kurie valentiniai ryšiai, ir jis ruošiasi tolesniam katalitiniam kitimui, o fermento molekulėje įvyksta konformaciniai persitvarkymai.
Košlando hipotezė, paremta aktyvaus fermento centro lankstumo teze, patenkinamai aiškino fermentų veikimo aktyvavimą ir inhibiciją ir jų aktyvumo reguliavimą veikiant įvairiems faktoriams. Šiuo metu Košlando hipotezė yra išstumiama topocheminio atitikimo hipotezės. Išsaugodama pagrindines Košlando teorijos tezes, ji fiksuoja tai, kad fermentų veikimo specifiką galima paaiškinti visų pirma tos substrato dalies, kuri nesikeičia vykstant katalizei, pažinimu. Tarp šios substrato dalies ir fermento substratinio centro įvyksta įvairios taškinės hidrofobinės sąveikos ir vandeniliniai ryšiai.
Fermentų klasifikacija ir nomenklatūra
Fermentologijoje ilgai neturėta griežtai mokslinės fermentų nomenklatūros. Trivialinės nomenklatūros pavyzdžiais galime pavadinti pepsiną, tripsiną, papainą. Pagal savo veikimo principą šie fermentai vadinami proteolitiniais, t. y., jie greitina proteinų hidrolizę. Labiausiai paplitusi yra racionalioji nomenklatūra, pagal kurią fermento pavadinimas sudaromas iš substrato pavadinimo ir galūnės "-azė". Ji buvo pasiūlyta 1883 m. E. Duclaux, Pastero mokinio. Fermentas, pagreitinantis krakmolo hidrolizės reakciją, buvo pavadintas amilaze, riebalų hidrolizę - lipaze.
Kai analitinės chemijos metodais buvo pasiekti tam tikri rezultatai prostetinių grupių iššifravimo srityje, atsirado nauja fermentų nomenklatūra. Juos ėmė vadinti pagal prostetinės grupės pavadinimą, pavyzdžiui, geminfermentas (prostetinė grupė - gem), piridoksal-fermentas (prostetinė grupė - piridoksal). Vėliau fermento pavadinime imta nurodyti ne tik substrato charakterį, bet ir katalizuojamos reakcijos tipą. Pavyzdžiui, fermentas, atimantis iš gintaro rūgšties molekulės vandenilį, vadinamas sukcinato dehidrogenaze.
1961 metais Tarptautinė fermentų nomenklatūros komisija pateikė nomenklatūros, grįstos griežtai moksliniais principais, projektą. Pagal ją fermento pavadinimas susideda iš cheminio substrato pavadinimo ir fermento vykdomos reakcijos pavadinimo. Pavyzdžiui, piridoksalfermentas, katalizuojantis peraminavimo reakciją tarp L-alanino ir α-ketoglutaro rūgšties, vadinasi L-alaninas: 2-oksoglutaro aminotransferazė. Šiame pavadinime pažymėti visi trys požymiai: 1) substratas yra L-alaninas; 2) akceptorius - 2-oksoglutaro rūgštis; 3) aminogrupė persiduoda nuo substrato prie akceptoriaus.
Fermentų pavadinimai pagal mokslinę nomenklūrą yra kur kas tikslesni, bet kartais tampa sudėtingesni už senuosius trivialius. Ryšium su žymių mokslinių pavadinimų sudėtingėjimu, naujoje nomenklatūroje leidžiama vartoti ir senus trivialinius pavadinimus.
Tarptautinė komisija sudarė detalų visų tuo metu žinomų fermentų sąrašą, papildytą 1972 metais, peržiūrint kai kurių fermentų nomenklatūrą ir klasifikaciją, kur šalia mokslinio pavadinimo duodamas ir senasis, o taip pat nurodomas fermento katalizuojamos reakcijos chemizmas ir kai kuriais atvejais fermento prigimtis. Kiekvienam fermentui suteiktas individualus numeris (šifras). Pavyzdžiui, ureazės šifras - 3.5.1.5. Tai reiškia, kad ureazė yra 3 klasės fermentas (hidrolazės), kurie katalizuoja hidrolizės reakcijas. Antras skaičius - 5 reiškia, kad ureazė priklauso 5 poklasei tos klasės, kuriai priklauso visi fermentai, pagreitinantys C-N ne peptidinių ryšių hidrolizę. Aukščiau minėta laktatdehidrogenazė turi 1.1.1.27, tai yra priklauso 1 klasės fermentams (oksidoreduktazės), 1 poklasei (oksioreduktazės, veikiančios CH-OH grupes kaip vandenilio atomų donorai), 1 papoklasei (vandenilio atomų akceptorius yra NAD(P)).
Automobilių katalizatoriai
Automobilių katalizatorius yra svarbi išmetimo sistemos dalis. Jis neutralizuoja kenksmingas dujas ir sumažina jų kiekį.
Nuo 1993 metų Europoje įsigaliojo teršalų išmetimo standartas. Šis standartas įpareigojo automobilių gamintojus diegti katalizatorius, kad jie galėtų sumažinti oro taršą. Šie prietaisai mažina šiltnamio efektą sukeliančias dujas ir gerina variklio efektyvumą.
Toliau šiame straipsnyje bus apžvelgtos katalizatorių veikimo principai, sandara ir priežiūros subtilybės. Tai padės geriau suprasti šio automobilio dalies svarbą.
Kas yra katalizatorius ir jo paskirtis automobilyje
Katalizatorius yra svarbi automobilio dalis, sukurta XX amžiaus viduryje. Jis padeda sumažinti šalutinių medžiagų išmetimus į aplinką. Pirmieji automobiliai su katalizatoriais pasirodė 1986 metais Europoje.
Šis įrenginys neutralizuoja anglies oksidus ir angliavandenilius. Jis taip pat sumažina azoto oksidų kiekį benzininiuose varikliuose. Dyzeliniuose varikliuose katalizatorius sumažina anglies oksidų, angliavandenilių ir kietųjų dalelių kiekį.
Katalizatoriaus atsiradimo istorija
Katalizatorius tapo būtina transporto priemonių įranga, kad atitiktų „Euro” išmetamųjų dujų standartus. Jis leido žymiai sumažinti automobilių neigiamą poveikį aplinkai.
Pagrindinės funkcijos transporto priemonėje
Katalizatorius veikia kaip tarpininkas, pagreitinantis chemines reakcijas. Jis mažina toksiškas medžiagas išmetamosiose dujose. Jis suaktyvina molekulių susidūrimus ir palengvina jų suskaidymą. Taip padeda sumažinti teršalų kiekį, išleidžiamą į aplinką.
Aplinkosauginė reikšmė
Katalizatoriai yra svarbūs kovai su oro tarša. Jų naudojimas ypač svarbus miestų centruose. Tinkamai veikiantys katalizatoriai padeda išvengti žalingo poveikio žmonių sveikatai.
Katalizatoriaus sandara ir pagrindiniai komponentai
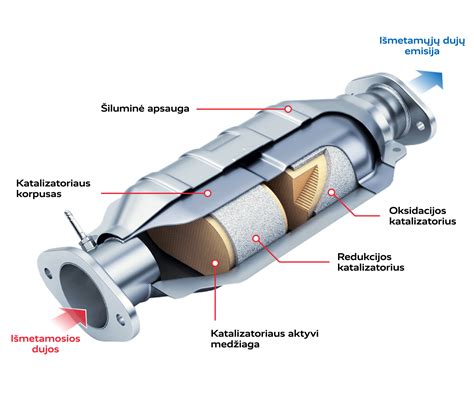
Kiekvienas katalizatorius susideda iš keturių pagrindinių dalių: korpusas, karkasas, tarpinis sluoksnis ir aktyviojo katalitinio sluoksnis. Kiekvienas šis elementas yra būtinas, kad katalizatorius efektyviai veiktų.
- Korpusas - metalinis bakelis, kuris saugo katalizatorių nuo perkaitimo.
- Karkasas - pagrindas, per kurį dujos pereina.
- Tarpinis sluoksnis - apsaugo aktyvųjį sluoksnį nuo mechaninių pažeidimų.
- Aktyvusis katalitinis sluoksnis - pagrindinis veiksmo centras. Jis pagamintas iš specialių medžiagų, kurios šalina dujas, kaip anglies monoksidas.
Kiekvienas komponentas kartu prisideda prie katalizatoriaus efektyvumo ir regeneracijos. Jie visi padeda išmetamųjų dujų valymui ir draugiškesnei aplinkai.
Cheminiai procesai katalizatoriuje
Katalizatoriuje vyksta trys pagrindinės cheminės reakcijos. Jis vadinamas trijų reakcijų katalizatoriumi. Oksidacijos ir redukcijos efektyvumas priklauso nuo jo gebėjimo pasisavinti deguonį.
Šių katalizės reakcijų metu kenksmingos dujos virsta nekenksmingomis. N2, H2O ir CO2 dujos tampa svarbios.
Oksidacijos ir redukcijos reakcijos
Katalizatoriuje vyksta sudėtingi cheminiai procesai. Vienu metu vienos medžiagos oksiduojamos, kitos redukuojamos. Šioje temperatūroje cheminiai procesai vyksta geriausiai. Tai garantuoja gerą katalizės reakcijų rezultatą.
Deguonies mainų mechanizmai
Katalizatoriaus efektyvumas priklauso nuo jo gebėjimo pasisavinti deguonį. Šie katalizės mechanizmai yra svarbūs. Jie padeda sumažinti kenksmingų medžiagų kiekį.
Benzininių ir dyzelinių katalizatorių skirtumai
Katalizatorių technologija ir savybės yra labai svarbios automobilių pramonei. Jie padeda mažinti dujų taršą, kurią išmeta transporto priemonė. Benzininiai ir dyzeliniai katalizatoriai skiriasi, kadangi pasižymi unikaliomis savybėmis.
- Benzininiai katalizatoriai vadinami „trijų funkcijų” dėl savo veiksmo. Jie neutralizuoja anglies monoksidą, angliavandenilius ir sumažina azoto oksidų kiekį. Tai svarbu mažinant miesto taršą.
- Dyzelinių katalizatoriai labiau koncentruojasi į anglies monoksido, angliavandenilių ir kietųjų dalelių sumažinimą. Dėl dyzelinių variklių specifikos, šiems katalizatoriams reikia papildomo kietųjų dalelių filtro ir SCR sistemos.
Naujuose automobilių modeliuose dažnai naudojami keli katalizatoriai. Jie padeda užtikrinti didžiausią išmetamųjų dujų valymą ir atitikti aplinkosaugos standartus.
Katalizatorių tipai ir jų ypatybės
Automobilių išmetamosiose dujose esančius teršalus šalina įvairių tipų katalizatoriai. Pagrindinės dvi kategorijos yra metaliniiai ir keramikiniai katalizatoriai. Jie skiriasi savo savybėmis ir pritaikymu.
Metaliniai katalizatoriai
Metaliniai katalizatoriai pasižymi greitesne darbine temperatūra. Jie atsparūs mechaniniams pažeidimams ir atlaiko iki 1300°C temperatūrą. Šie katalizatoriai yra efektyvesni ir leidžia greičiau sumažinti išmetamųjų dujų teršalus.
Keramikiniai katalizatoriai
Keramikiniai katalizatoriai atlaiko aukštesnę temperatūrą nei daugelis medžiagų, tačiau nepasiekia metalinių katalizatorių darbinės temperatūros (veikia iki 800°C). Jie yra mažiau patvarūs, tačiau pigiau pagaminami.
Kiekvieno tipo katalizatorius turi savų privalumų ir tinka konkrečioms transporto priemonėms.
Katalizatoriaus veikimo principai
Katalizatorius pradeda veikti, kai jo temperatūra pasiekia 300°C. Deguonies jutikliai stebi degalų ir oro santykį. Jie perduoda šią informaciją į variklio kompiuterį.
Variklio kompiuteris reguliuoja degalų įpurškimą, tad palaiko optimalų degalų ir oro mišinį. Tai svarbu katalizatorių efektyvumui.
Katalizatoriuje vyksta katalizės mechanizmai. Jie sumažina teršalų kiekį. Procesai apima oksidacijos ir redukcijos reakcijas, kurios reikalauja deguonies.
Temperatūros svyravimai gali turėti įtakos katalizatorių efektyvumui - žema temperatūra lėtina vykstančias reakcijas, o per aukšta gali pažeisti patį katalizatorių. Deguonies jutikliai užtikrina optimalų degalų ir oro mišinį, reikalingą efektyviems katalizės mechanizmams.
Tinkamas katalizatoriaus veikimas pagerina išmetamųjų dujų kokybę ir sumažina kenksmingų medžiagų išsiskyrimą į aplinką.
Dažniausios gedimo priežastys ir požymiai
Katalizatoriai gali gesti dėl daugelio priežasčių. Smūgiai ir deformacijos labai kenkia jų veikimui. Netinkamai sureguliuotos dujinės įrangos ir uždegimo sistemos gedimai taip pat yra problemos.
Stūmoklių žiedai, žvakės, nepakankamai keičiamas oro filtras ir nekokybiškas kuras taip pat gali sukelti problemas. Šie veiksniai lemia prastesnį automobilio veikimą, padidina kuro sąnaudas ir pasireiškia „Check engine” įspėjamąja lempute.
Mechaniniai pažeidimai
Automobilių katalizatorių vagystės padažnėjusios, kai katalizatoriai išpjaunami kaip vertingų metalų šaltinis. Katalizatoriai gali būti mechaniškai pažeidžiami įvažiuojant į kelkraščius, smarkiai įvažiuojant į duobes ar apvažiuojant kliūtis. Netinkamas katalizatoriaus išmontavimas ar montavimas taip pat gali jį sugadinti.
Eksploataciniai gedimai
Katalizatorius laikomas patvariu komponentu. Tačiau ilgai nekeičiamas oro filtras, nekokybiški tepalai ar kuras, uždegimo sistemos gedimai ir kitos priežastys gali sukelti problemas. Dažniausi simptomai - barškėjimas, sumažėjusi variklio galia, padidėjusios kuro sąnaudos ir „Check engine” lemputės įsijungimas.
Reguliari katalizatoriaus priežiūra, įskaitant periodišką valymą ir stebėjimą, padeda palaikyti jo efektyvumą. Svarbu taip pat užtikrinti tinkamą kuro sistemų, uždegimo ir kitų komponentų veikimą, kad katalizatorius būtų apkraunamas optimaliomis sąlygomis.
Katalizatoriaus priežiūra ir eksploatacija
Norint prailginti katalizatoriaus tarnavimo laiką, būtina tinkamai prižiūrėti šią transporto priemonės dalį. Katalizatorių efektyvumas gali būti išlaikomas iki 180-200 tūkstančių km, tačiau tai reikalauja laikytis tam tikrų rekomendacijų:
- Vengti mechaninių pažeidimų - svarbu saugoti katalizatorių nuo didelių smūgių ir vibracijos.
- Naudoti tik kokybišką kurą - prastos kokybės degalai gali sukelti katalizatoriaus užsikimšimą.
- Reguliariai keisti oro filtrą - užsiteršęs filtras gali sutrikdyti tinkamą oro tiekimą į variklį.
- Tinkamai prižiūrėti uždegimo sistemą - netinkamai sureguliuota uždegimo sistema gali padidinti kenksmingų medžiagų išmetimą į katalizatorių.
- Vengti dažno važinėjimo trumpais atstumais mieste ir netinkamo dujinės įrangos sureguliavimo. Tai gali sutrumpinti katalizatoriaus eksploatacijos laiką.
Reguliari katalizatorių priežiūra ir tinkama eksploatacija padeda išlaikyti optimalią šios sistemos būklę.
Vertingieji metalai katalizatoriuose ir perdirbimas
Katalizatoriuose naudojami reti ir brangūs cheminiai elementai, kaip platina, rodys ir paladis. Dėl to katalizatoriai yra vertingi perdirbimui. Net ir neveikiantis katalizatorius gali būti parduotas antriniam naudojimui, suteikiant jam antrą gyvenimą.
Vertingųjų metalų kiekis katalizatoriuje priklauso nuo jo modelio, eksploatacijos laiko ir šalies reikalavimų. Pavyzdžiui, automobilių katalizatoriai gali turėti nuo 2 iki 7 gramų platinos, rodžio ir paladžio. Pramoniniai katalizatoriai gali turėti daugiau.
Šių metalų perdirbimas padeda išgauti ir panaudoti juos pakartotinai, užtikrinant tvarų katalizatorių naudojimą įvairiose industrijose. Katalizatorių perdirbimo procesas yra sudėtingas, tačiau svarbus siekiant mažinti priklausomybę nuo ribotų gamtinių išteklių.
[HINDI] Katalizatorius: Veikimas | Animacija | Dviejų pakopų
tags: #kuo #skiriasi #fermentas #nuo #katalizatoriaus
