Gyvojo pasaulio pagrindinis skiriamasis bruožas yra nuolatinis jį sudarančių medžiagų kitimas - apykaita. Medžiagos nuolat skyla ir vėl susidaro, o tai susiję su cheminėmis reakcijomis. Gyvoje ląstelėje šios reakcijos vyksta labai švelniomis sąlygomis: temperatūra ne aukštesnė nei 40°C, o vandens terpės pH yra tarp 6,5 ir 7,5. Kolboje tokiomis sąlygomis dauguma reakcijų vyktų labai lėtai arba visai nevyktų. Būtent todėl gamta sukūrė specialius junginius, kurie pagreitina šiuos procesus - fermentus.
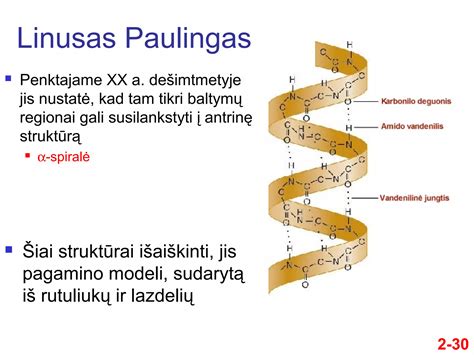
Kas yra fermentai?
Fermentai, arba enzimai, yra biologiniai katalizatoriai. Tai - junginiai, greitinantys organizme vykstančias chemines reakcijas, tačiau patys jose nesunaudojami ir nepagaminami. Beveik visos cheminės reakcijos organizme vyksta, dalyvaujant šiems biologiniams katalizatoriams. Jei ląstelėse jų nebūtų, cheminės reakcijos vyktų labai lėtai (keliolika valandų, mėnesių) arba netgi visai nevyktų, todėl tokios ląstelės negalėtų egzistuoti.
Daugelis fermentų yra baltymai, priklausantys baltymų organinių molekulių grupei. Jie pasižymi dideliu aktyvumu ir užtikrina visus gyvybinius procesus, reguliuodami tiek sintezės, tiek skilimo reakcijas ir palaikydami organizmo metabolizmą.
Fermentų veikimo principas: substratas ir produktas
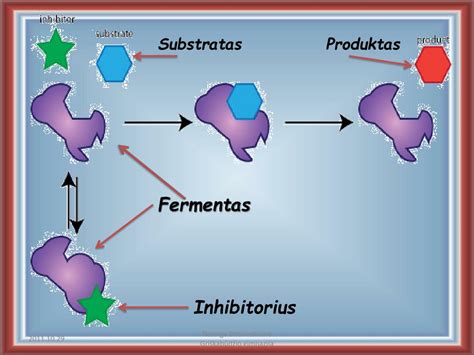
Fermentinės reakcijos metu, cheminis junginys, prie kurio prisijungia fermentas ir kurio virsmus katalizuoja, yra vadinamas substratu. Substratai - tai pradinės medžiagos, dalyvaujančios fermentinėse reakcijose. Po reakcijos susidaręs naujas junginys vadinamas produktu.
Fermentai turi specifinę sritį, vadinamą aktyviuoju centru. Tai nedidelė fermento dalis, kuri sąveikauja su specifine chemine dalebėle, t. y. substratu. Substratas prisijungia prie fermento aktyviojo centro ir su juo sudaro fermento ir substrato kompleksą. Ši sąveika dažnai apibūdinama kaip „raktas spynai“, pabrėžiant fermento ir substrato formos atitikimą.
Fermentų savybės: bendrosios ir specifinės
Bendrosios katalizatorių savybės
Fermentai, kaip ir kiti katalizatoriai, pasižymi šiomis bendrosiomis savybėmis:
- Reakcijos metu jie nei sunaudojami, nei pagaminami, todėl gali būti panaudoti daug kartų.
- Jie didina reakcijos greitį.
- Jie nekeičia reakcijos pusiausvyros. Fermentai katalizuoja tiek tiesioginę, tiek atvirkštinę reakciją, padėdami greičiau pasiekti pusiausvyrą, bet nepakeisdami jos padėties.
Specifinės fermentų savybės
Be bendrųjų katalizatorių savybių, fermentams būdingos ir specifinės savybės, kurios juos išskiria:
- Specifiškumas: Fermentai yra labai specifiški - jie greitina tik tam tikrą cheminę reakciją ir negamina šalutinių reakcijos produktų. Kiekvienas fermentas valdo tik tam tikrą cheminę reakciją, nes substrato forma turi atitikti fermento aktyvųjį centrą, kaip raktas spyną. Kai kurie fermentai yra griežtai specifiški vienam substratui, o kiti gali katalizuoti keleto panašių junginių virsmus.
- Jautrumas sąlygoms: Fermentai yra jautrūs aplinkos pokyčiams, ypač temperatūrai ir terpės rūgštingumui (pH). Nukrypimas nuo optimalių sąlygų gali sumažinti arba visiškai inaktyvuoti fermento veiklą.
- Reguliuojamumas: Fermentų aktyvumas yra reguliuojamas. Tai reiškia, kad jų veikla priklauso nuo tam tikrų junginių kiekio ląstelėje, leidžiančio organizmui kontroliuoti reakcijų greitį pagal poreikius.
- Kofaktoriai ir kofermentai: Be baltyminės dalies, į fermento sudėtį dažnai įeina ir nebaltyminės prigimties komponentai. Tai gali būti mažos molekulinės masės medžiagos, vadinamos kofermentais (dažniausiai vitaminų dariniai) arba prostetinėmis grupėmis. Kofermentai arba mineralai, vadinami kofaktoriais (pvz., geležies, cinko, magnio ar kalcio jonai), yra absoliučiai būtini daugeliui fermentų, nes be jų fermentas negali funkcionuoti. Apofermento (baltyminės dalies) ir kofaktoriaus kompleksas vadinamas holofermentu - aktyvia fermento forma.
Kaip fermentai spartina reakcijas? Aktyvacijos energijos mažinimas
Cheminės reakcijos įvyksta tik susidūrus molekulėms, kurių ne tik energija yra pakankamai didelė, bet ir erdvinė padėtis yra palanki. Kiekvienai reakcijai yra būdinga tam tikra laisvosios energijos užtvara, kurią įveikia ne visos, bet tik pakankamai aktyvios molekulės. Tokių molekulių būsena vadinama aktyviąja, arba pereinamąja, būsena. Fermentai didina reakcijos greitį mažindami šią energijos užtvarą, vadinamą aktyvacijos energija.
Fermentai mažina reaguojančių medžiagų standartinę laisvąją aktyvacijos energiją (∆G°‡), t. y. reakcijos energijos užtvarą, nes jie padidina skaičių tokių substrato molekulių, kurioms pakanka energijos pasiekti pereinamąją būseną. Dėl to, esant fermentams, vienodai didėja ir tiesioginės, ir grįžtamosios reakcijų greičiai, tačiau nekinta substratų ir produktų standartinės laisvosios energijos pokytis ir reakcijos pusiausvyros konstanta.
Fermentų įtaka aktyvacijos energijai pasireiškia per kelis mechanizmus:
- Entalpijos (∆H°‡) mažinimas: Fermentas mažina reakcijos entalpiją sukurdamas keletą tarpinių substrato būsenų. Kiekviena iš šių būsenų yra nepatvari, todėl greitai virsta kita ir galiausiai reakcijos produktu. Tarpinių substrato būsenų energija yra mažesnė už pereinamosios būsenos energiją, todėl sumažėja fermentinės reakcijos energijos užtvara.
- Entropijos (∆S°‡) didinimas: Reaguojančių molekulių tarpusavio erdvinė padėtis yra labai svarbi, kad įvyktų cheminė reakcija. Fermentai prisijungia substratus taip, kad jų erdvinė padėtis būtų palankiausia reakcijai įvykti. Taigi fermentas sumažina aktyvacijos entropijos neigiamą dydį (t. y., didina ∆S), taip padidindamas sėkmingų susidūrimų tikimybę.
Fermentinių reakcijų greitis ir jį veikiantys veiksniai
Substrato arba produkto koncentracijos pokytis per laiko vienetą vadinamas cheminės reakcijos greičiu. Fermentinių reakcijų greitį ir fermentų veikimą veikia šie veiksniai:
- Temperatūros įtaka: Kiekvienas fermentas turi optimalią temperatūrą, kurioje jo aktyvumas yra didžiausias. Per didelė temperatūra gali sukelti baltymo denatūraciją ir negrįžtamą fermento aktyvumo praradimą.
- pH įtaka: Terpės rūgštingumas (pH) taip pat turi didelę įtaką fermento aktyvumui. Fermentai geriausiai veikia tam tikrame pH diapazone, atspindinčiame jų natūralią aplinką (pvz., virškinimo fermentai skrandyje veikia rūgščioje terpėje, žarnyne - šarminėje).
- Fermento koncentracijos įtaka: Kuo didesnė fermento koncentracija, tuo daugiau aktyviųjų centrų yra prieinama substratui, ir tuo didesnis reakcijos greitis (iki tam tikros ribos).
- Substrato koncentracijos įtaka: Didėjant substrato koncentracijai, reakcijos greitis didėja, kol visi aktyvieji fermentų centrai yra užimti. Pasiekus soties tašką, toliau didinant substrato koncentraciją, reakcijos greitis nebedidėja.
Fermentų reikšmė gyvybiniuose procesuose ir medicinoje
Be fermentų neapsieina nė vienas organizme vykstantis procesas - kvėpavimas, virškinimas, judėjimas, augimas, vystymasis ir kt. Jie atlieka daugybę sudėtingų ląstelės biologinių funkcijų, pavyzdžiui, energijos aprūpinimą.
Medicinos praktikoje fermentų veikimo principų žinojimas yra labai svarbus, kadangi jie reguliuoja visą medžiagų apykaitą, o daugelis susirgimų yra susiję su medžiagų apykaitos sutrikimais.
- Virškinimas: Virškinimo trakto sutrikimams gydyti naudojami proteazių, amilazių bei lipazių mišiniai. Pavyzdžiui, amilazė skaido angliavandenius, transformuodama juos į gliukozę, ir pradeda veikti jau burnos ertmėje su seilėmis. Lipazė perdirba ir skaido riebalus, padėdama įsisavinti riebaluose tirpius vitaminus. Laktazė iš pieno cukraus (laktozės) transformuoja jį į gliukozę ir galaktozę; šio fermento trūkumas sukelia laktozės netoleravimą.
- Antioksidacinė apsauga: Superoksiddismutazė - tai fermentas, kuris greitina superoksido anijono dismutaciją ir neutralizuoja šio aktyvaus deguonies neigiamą poveikį organizmui. Katalazė, kurios ypač daug kepenyse, inkstuose ir kraujyje, greitina toksinio vandenilio peroksido skilimą į vandenį ir deguonį. Peroksidazės katalizuoja oksidacijos reakcijas, padedant vandenilio peroksidui.
- Terapinės paskirties fermentai: Įvairios kilmės lizuojantys fermentai ir proteazės tirpina krešulius kraujagyslėse. Asparaginazės ir gliutaminazės naudojamos gydant leukozes.
- Augalinės kilmės fermentai: Papainas, randamas ananasuose ir papajose, skaido baltymus, riebalus ir angliavandenius, palengvindamas jų įsisavinimą. Jis aktyvus įvairiose terpėse. Bromelainas, randamas ananasuose, pasižymi priešuždegiminiu poveikiu, mažina kraujo krešumą ir gerina virškinimą.
tags: #kodel #fermentai #vadinami #biologiniais #katalizatoriais
